Các phương pháp miễn dịch “không đặc hiệu” trước đây như cytokine (interleukin-2, interferon-α), vaccine ung thư, hay virus oncolytic cho thấy hiệu quả khiêm tốn và tính ứng dụng hạn chế. Cho đến khi cơ chế điều hòa miễn dịch qua các "điểm kiểm soát" (immune checkpoints) được khám phá nhờ thành tựu của 2 nhà khoa học James P. Allison và Tasuku Honjo – được vinh danh bằng Giải Nobel Y học năm 2018 – nền y học ung thư mới thực sự bước sang một trang mới. Khám phá này mở đường cho sự phát triển của các chất ức chế điểm kiểm soát miễn dịch (Immune Checkpoint Inhibitors - ICI), làm thay đổi diện mạo điều trị cho nhiều loại bệnh ung thư.

Hình 1: The Nobel Prize in Physiology or Medicine 2018. NobelPrize.org
*Cơ chế tác động
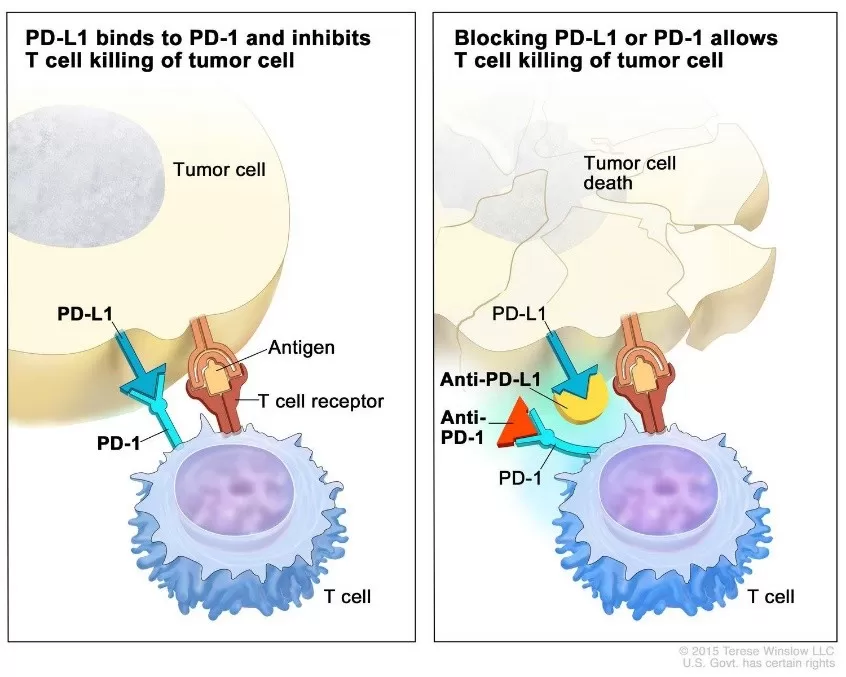
Trong điều kiện sinh lý bình thường, hệ miễn dịch của cơ thể tự thiết lập các cơ chế "kiểm soát" tinh vi, như các phân tử CTLA-4 và PD-1/PD-L1, để ngăn chặn phản ứng tự miễn và bảo vệ các mô lành. Tế bào ung thư đã lợi dụng cơ chế này để làm giảm khả năng nhận diện của hệ thống miễn dịch với tế bào u thông qua sự gắn kết giữa các phối tử PD-L1 trên tế bào u và thụ thể PD-1 trên tế bào T. Bằng cách tăng biểu hiện quá mức phối tử PD-L1 trên bề mặt, chúng liên kết với thụ thể PD-1 trên tế bào T, làm vô hiệu hóa hay “làm mù” khả năng tiêu diệt khối u của tế bào T.
Các thuốc ICI hoạt động như một "chìa khóa" để phong tỏa các tương tác ức chế này. Bằng cách ức chế con đường PD-1/PD-L1 hoặc CTLA-4, các thuốc miễn dịch giải phóng, tái kích hoạt chức năng của tế bào T và cho phép chúng tấn công khối u một cách mạnh mẽ và bền bỉ. Các nhóm thuốc chính bao gồm:
- Ức chế PD-1: Nivolumab, Pembrolizumab.
- Ức chế PD-L1: Atezolizumab, Durvalumab, Avelumab.
- Ức chế CTLA-4: Ipilimumab (thường được sử dụng phối hợp với thuốc ức chế PD-1).
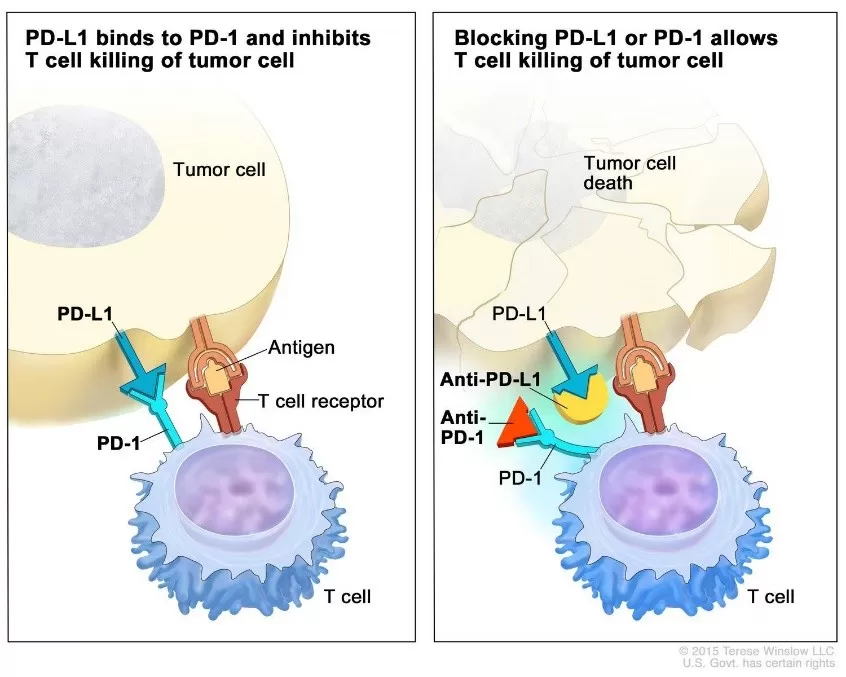
Hình 2: National Cancer Institute. Immune Checkpoint Inhibitors to Treat Cancer. NCI Visuals Online
Nhờ cơ chế tác động độc đáo này, ICI có khả năng tạo ra các đáp ứng lâm sàng kéo dài, một kết quả hiếm khi đạt được với các liệu pháp cổ điển.
Phác đồ và Chiến lược Ứng dụng Lâm sàng
- Đường dùng và Chu kỳ: Các thuốc ICI chủ yếu được truyền qua đường tĩnh mạch với chu kỳ 2-4 tuần/lần. Xu hướng mới có thể có sản phẩm tiêm dưới da nhằm tối ưu hóa thời gian và trải nghiệm điều trị cho bệnh nhân.
- Liệu pháp phối hợp: Để tối đa hóa hiệu quả, ICI thường được nghiên cứu và ứng dụng trong các phác đồ phối hợp đa mô thức với hóa trị, xạ trị, liệu pháp nhắm trúng đích, và thậm chí với các ICI khác (ví dụ: ipilimumab + nivolumab).
- Thời gian điều trị: Thời gian điều trị tuỳ thuộc vào mục tiêu điều trị, giai đoạn bệnh (điều trị củng cố/bổ trợ trong giai đoạn sớm hay giai đoạn tiến triển tại vùng; điều trị tân bổ trợ trước phẫu thuật…). Với giai đoạn di căn, bệnh nhân có thể cần điều trị kéo dài lên tới 2 năm hoặc điều trị liên tục đến khi bệnh không đáp ứng hoặc xuất hiện tác dụng phụ nghiêm trọng.
Chỉ Định và Lựa Chọn Bệnh Nhân:
ICI hiện đã trở thành điều trị tiêu chuẩn cho nhiều loại bệnh ung thư, bao gồm:
- Ung thư phổi không tế bào nhỏ (NSCLC)
- U hắc tố (Melanoma)
- Ung thư đầu cổ (Head & Neck Cancer)
- Ung thư thực quản (Esophageal cancer)
- Ung thư dạ dày (Gastric cancer)
- Ung thư đại trực tràng (Colorectal cancer)
- Ung thư biểu mô tế bào thận (RCC)
- Ung thư biểu mô đường tiết niệu (Urothelial Carcinoma)
- Ung thư gan nguyên phát (HCC)
- Các khối u đặc có trạng thái MSI-H/dMMR hoặc TMB cao (Tumor Mutational Burden)
Việc lựa chọn bệnh nhân phù hợp là yếu tố then chốt. Các xét nghiệm sinh học như đo lường mức độ biểu hiện PD-L1 (bằng IHC), đánh giá tình trạng MSI-H/dMMR, hoặc xác định khối lượng đột biến khối u (TMB) đóng vai trò là các chất chỉ điểm tiên lượng quan trọng, giúp cá thể hóa liệu pháp và tối ưu hóa cơ hội đáp ứng.
Cân bằng giữa lợi ích và nguy cơ
Lợi ích:
- Cải thiện tỷ lệ thời gian sống thêm bệnh không tái phát sau điều trị phẫu thuật triệt căn (DFS - Disease-free Survival), thời gian sống thêm bệnh không tiến triển (Progression-free Survival), thời gian sống thêm toàn bộ (Overall Survival - OS) ở nhiều nhóm bệnh ung thư.
- Khả năng đạt được đáp ứng lâu dài, thậm chí là lui bệnh hoàn toàn ở một nhóm bệnh nhân.
- Phổ tác dụng phụ khác biệt, ít gây các độc tính phổ biến của hóa trị như ức chế tủy xương, rụng tóc hay buồn nôn nghiêm trọng.
Nguy cơ (Biến cố bất lợi liên quan đến miễn dịch - irAEs):
Việc giải phóng hoạt động của hệ miễn dịch có thể dẫn đến các phản ứng tự miễn, gây viêm và tổn thương các cơ quan bình thường. Các irAEs có thể ảnh hưởng đến bất kỳ cơ quan nào, phổ biến nhất bao gồm:
- Viêm phổi (Pneumonitis)
- Viêm đại tràng (Colitis)
- Viêm gan (Hepatitis)
- Rối loạn nội tiết (Viêm tuyến giáp, viêm tuyến yên, viêm tụy)
- Các biểu hiện ngoài da (ban đỏ, ngứa)
- Mệt mỏi
Phần lớn các irAEs có thể được kiểm soát hiệu quả bằng cách phát hiện sớm, theo dõi sát sao, và can thiệp kịp thời với corticosteroid hoặc các thuốc ức chế miễn dịch khác (như infliximab cho các trường hợp nặng).
Hành trình ứng dụng ICI tại Việt Nam:
Tại Việt Nam, các thuốc ICI (Pembrolizumab, Atezolizumab, Durvalumab) đã chính thức được Bộ Y tế phê duyệt và đưa vào sử dụng. Tuy chưa được thanh toán BHYT, song với các chương trình viện trợ một phần chi phí thuốc (các chương trình PAP) hiện đang được các nhà tài trợ phối hợp các bệnh viện áp dụng thực hiện, giúp giảm bớt gánh nặng tài chính cho người bệnh, từ đó tăng khả năng tiếp cận phương pháp điều trị mới nhiều ưu việt này.
Bệnh viện Ung Bướu Hà Nội đã triển khai điều trị miễn dịch cho hàng trăm bệnh nhân ung thư, đặc biệt cho các ung thư phổi, gan, u hắc tố và ung thư đầu cổ. Bên cạnh đó, Bệnh viện luôn cập nhật phác đồ điều trị theo các hướng dẫn quốc tế uy tín (NCCN, ESMO) và tích cực tham gia các nghiên cứu lâm sàng đa trung tâm, tiếp cận các phương pháp điều trị ung thư mới (thuốc phức hợp kháng thể-thuốc ADC, kháng thể đặc hiệu kép bispecific…).
Theo dõi và Quản lý bệnh nhân: Quy trình chặt chẽ và toàn diện
- Trước điều trị: Đánh giá toàn diện bao gồm chức năng các cơ quan (tim mạch, gan, thận, phổi, tuyến nội tiết) và các xét nghiệm chất chỉ điểm sinh học.
- Trong điều trị: Theo dõi sát sao lâm sàng và cận lâm sàng định kỳ để đánh giá đáp ứng và phát hiện sớm các irAEs. Các đánh giá bằng chẩn đoán hình ảnh (CT, PET-CT) được thực hiện theo chu kỳ.
- Sau điều trị: Cần cảnh giác với các biến chứng muộn, vì irAEs có thể khởi phát thậm chí sau khi đã ngừng thuốc. Giáo dục cho bệnh nhân và người nhà nhận biết các triệu chứng báo động (sốt, khó thở, tiêu chảy, vàng da, mệt mỏi cực độ) là vô cùng quan trọng.
Kết luận
Liệu pháp ức chế điểm kiểm soát miễn dịch (ICI) đại diện cho một trong những bước tiến quan trọng của ung thư học trong thập kỷ vừa qua, mở ra kỷ nguyên mới của điều trị cá thể hóa và mang lại hy vọng sống còn cho vô số bệnh nhân. Tuy nhiên, đây không phải là một liệu pháp phù hợp với mọi đối tượng bệnh nhân. Việc chỉ định cần được cân nhắc thận trọng bởi các bác sĩ chuyên khoa ung bướu dựa trên đặc điểm bệnh học, giai đoạn bệnh, đặc điểm sinh học phân tử của khối u và tình trạng toàn thân của người bệnh.
Bệnh viện Ung Bướu Hà Nội, với vai trò bệnh viện tuyến đầu trong điều trị ung thư, cam kết không ngừng cập nhật, ứng dụng và làm chủ những liệu pháp tiên tiến nhất, cùng đội ngũ đa chuyên khoa giàu kinh nghiệm, nhằm mang đến cho người bệnh ung thư Việt Nam cơ hội được tiếp cận với những phương pháp điều trị tối ưu nhất.
Tài liệu Tham khảo
1. National Cancer Institute. Immunotherapy to Treat Cancer.
2. Cancer.Net (ASCO). What Is Immunotherapy?
3. The Nobel Prize in Physiology or Medicine 2018. NobelPrize.org.
Haanen, J.B.A.G., et al. (2021). Management of toxicities from immunotherapy: ESMO Clinical Practice Guidelines. Annals of Oncology
Viết bài: Ths.BS. Trần Thanh Hà - Khoa Nội Tổng hợp Theo yêu cầu
Duyệt bài: ThS.BSCKII. Lê Thị Lệ Quyên - Khoa Nội Tổng hợp Theo yêu cầu